Petita guia per a la determinació de l’anió en minerals solubles en àcids mitjançant química analítica casolana
Pedro Mingueza
Malgrat que avui dia la determinació d’un mineral per mètodes d’analítica química pot semblar quasi anacrònic, en realitat, encara pot ser un recurs molt útil com a complement als moderns sistemes d’anàlisi actual (Raman, SEM, difracció…). La principal raó és que no és habitual tenir accés a l’instrumental necessari i, en la majoria dels casos, encarregar l’anàlisi d’un exemplar ens costarà temps i diners.
En aquest sentit, els socis del GMC, en certa manera, som uns privilegiats al poder gaudir del servei d’anàlisi del Grup, però el propòsit d’aquest article és donar un cop de mà per a poder fer una aproximació prèvia en la classificació dels nostres exemplars i que, almenys, ens pugui ajudar a discriminar aquells que val o no la pena portar a analitzar, a més de donar pistes al Servei d’anàlisi si finalment ens decidim a utilitzar-lo.
El conjunt de proves que es relacionaran en aquest document va encaminat únicament a determinar quin és l’anió que forma part de la mostra i que ens permetrà, en certa manera, determinar la classe/subclasse a la que pertany dins dels models habituals de classificació de sistemàtica mineral (Strunz o Dana). En qualsevol cas, hem de ser conscients que no és una determinació inequívoca i que, encara que en la majoria dels casos la conclusió del resultat coincidirà amb la realitat, pot passar que un exemplar contingui més d’un anió o que, degut a la composició de la mostra, ens emmascari el resultat amb una altra reacció no prevista.
Altre aspecte important és que aquestes proves només seran aplicables a aquells exemplars que tinguin una certa solubilitat en àcids. Un consell comú a totes les proves és, si és possible, polvoritzar la mostra al màxim ja que això facilitarà en gran mesura la seva dissolució. Un altre consell és tenir paciència amb el procés de dissolució, algunes substàncies es dissoldran molt lentament, així que no serà desgavellat deixar el procés de dissolució fins a un parell d’hores si aquest és molt lent. A la web Mineralienatlas podeu trobar informació sobre el comportament amb els àcids de cada espècie mineral. Per suposat, la solubilitat o no d’un exemplar en àcids o altres compostos és sempre una propietat d’ajuda en la classificació per si mateixa.
Per últim, abans de entrar en matèria, dir que totes les proves són realment casolanes i senzilles, i han estat provades amb èxit, i que el diferent material ha estat aconseguit per un baix cost en drogueries, farmàcies o botigues de productes químics una mica més especialitzades. Les proves no representaran cap perill per a la salut tenint en compte que, en la majoria de les ocasions, no caldrà fer servir més d’una gota de reactiu ni més d’un trosset de mostra molt inferior al mil·límetre.
Tal com si es tractés d’un receptari de cuina, com a primer punt, faig una relació dels productes químics necessaris per cobrir les proves relacionades:
- àcid clorhídric (HCl): en la majoria dels casos serà suficient amb el típic salfumant, que acostuma a tenir una concentració del 20%. És preferible un clorhídric amb una concentració superior en els casos en que el mineral presenta una solubilitat moderada.
- àcid nítric (HNO3) : drogueria o botiga de productes químics
- clorur de bari (BaCl2): botiga de productes químics
- molibdat amònic (H24Mo7N6O24): botiga de productes químics
- nitrat de plata (AgNO3): acostuma a ser car i, per la quantitat que es necessita, és més pràctic adquirir algun producte de farmàcia per a tractar berrugues o similars que porti nitrat de plata
- aigua oxigenada (H2O2)
- amoníac (NH3)
- fil de coure (Cu)
- aigua destil·lada (H2O)
En general, com a primera aproximació, podem dir que els minerals que contenen determinats anions acostumen a presentar bona solubilitat en àcids. Aquests compostos més comuns són els halogenurs, sulfats, carbonats, fosfats, arseniats i vanadats. Aquesta guia consistirà en la descripció d’una sèrie de proves, una per a cada tipus d’anió, que determinarà si té o no l’anió corresponent. L’ordre de les proves que apareix al document obeeix a una possible seqüència estratègica de determinació per minimitzar esforços quan no tenim cap pista del que pot ser el mineral a analitzar.
Alguns anions queden fora d’aquestes proves degut a que no s’ha pogut trobar cap prova senzilla i casolana per a la seva determinació o perquè els seus compostos es troben molt rarament a la natura. En tot cas, com a primera aproximació, pot ser suficient ja que queden inclosos aquells que presenten millor dissolució en àcids.
Proves:
1- Carbonats
És la prova més senzilla i coneguda. Consisteix en submergir un trosset de mostra en àcid clorhídric i veure si produeix efervescència a l’alliberar CO2 en la reacció
XCO3 + 2HCl → XCl2 +CO2+H2O
Resultarà molt aparent determinar que és un carbonat per aquells minerals molt solubles com és el cas de la calcita, la malaquita o l’atzurita. Hi ha d’altres que tenen una solubilitat més baixa i poden produir alguna bombolla aïllada que no ens permet assegurar que ho sigui. En aquests casos s’haurà de repetir la prova però amb el clorhídric calent, on la majoria dels carbonats faran una efervescència clara (dolomita, cerussita, rodocrosita, smithsonita…).
2- Silicats
Encara que no hi ha molts silicats que presentin una bona solubilitat en àcids, si la tenen, en molts casos, el silicat es pot detectar amb una bona observació. Fent la mateixa acció de submergir la mostra en clorhídric, veurem que, tal com aquesta es dissol, es va formant una espècie de residu granular, més aviat incolor, que no és més que gel de sílice (diòxid de silici més o menys hidratat) .
3- Arsenats
Com en els casos anteriors, submergim un trosset de mostra en àcid clorhídric. Una vegada s’ha dissolt una quantitat acceptable de la mostra, col·locarem un fil de coure sobre la dissolució. Si la mostra conté l’anió arsenat, al cap d’una estona la superfície del fil de coure s’anirà ennegrint. Això és degut que es diposita arsènic (negre) a les parets del coure per un procés redox. S’ha de tenir en compte que, independentment de que la dissolució tingui arsènic, en molts casos, al afegir el fil de coure, la dissolució es torna d’un color marró fosc. Això no serà cap indicador i només conclourem que és un arsenat si la superfície del coure es posa negre.

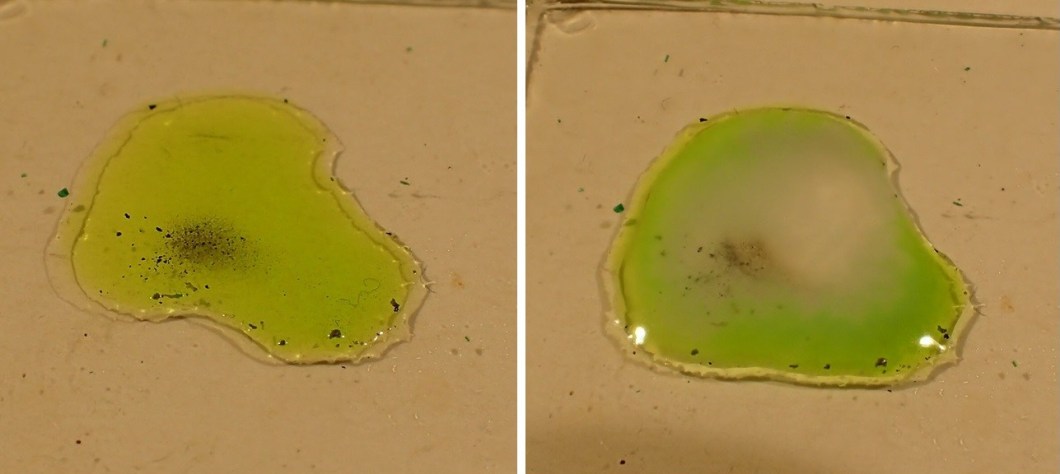
4- Vanadats
Igualment, submergim un trosset de mostra en àcid clorhídric. Una vegada s’ha dissolt una quantitat acceptable de la mostra, afegirem una gota d’aigua oxigenada a la dissolució. Si el resultat és positiu la solució es tornarà immediatament d’un color marró/vermell intens degut a la precipitació d’òxid de vanadi.
Aquesta prova es pot fer també amb àcid nítric (HNO3) en el cas que la mostra no tingui bona dissolució en àcid clorhídric (HCl), com és el cas de la vanadinita.

5- Sulfats
Com en els casos anteriors, submergim un trosset de mostra en àcid clorhídric (HCl). Seguidament prepararem una petita dissolució en aigua de clorur de bari (BaCl2). Finalment, deixarem anar una o dues gotes de la dissolució de BaCl2 sobre la dissolució de la mostra. Si com a resultat comença a aparèixer un precipitat de color blanc, voldrà dir que a la dissolució tenim l’anió sulfat, que amb la presencia del bari precipita a sulfat de bari donant el color blanc característic.
6- Fosfats
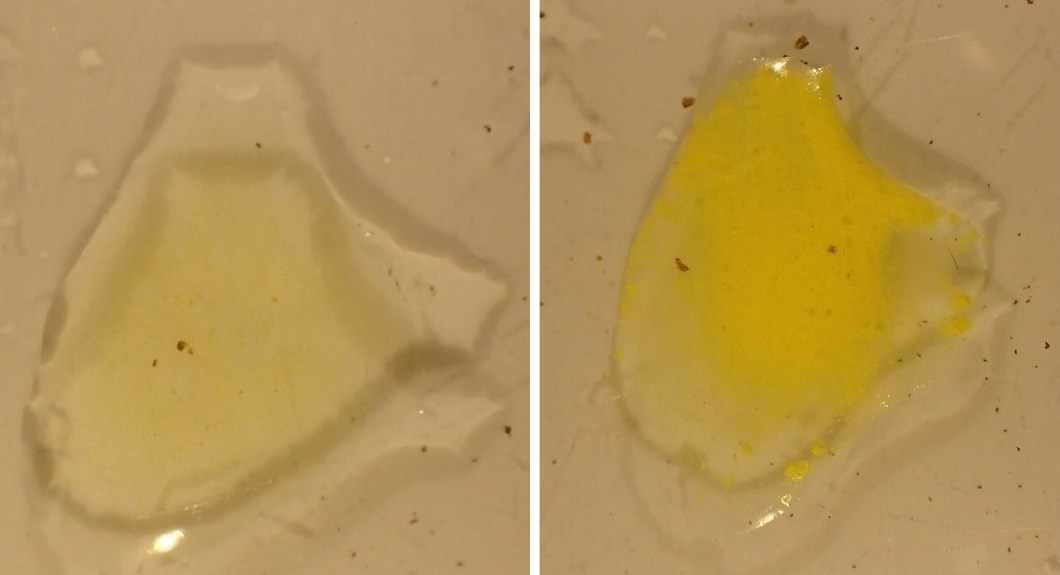
A diferència de les proves anteriors, en aquesta ocasió submergirem un trosset de mostra en àcid nítric (HNO3) fins que la mostra es dissolgui. Seguidament, prepararem una petita dissolució de molibdat amònic (H24Mo7N6O24) en aigua destil·lada. Finalment, afegirem una o dues gotes de la dissolució de molibdat amònic sobre la dissolució de la mostra. En el cas que en la dissolució de la mostra hi hagués l’anió fosfat (PO4–) la dissolució començarà a tornar-se d’un color groc canari intens degut a la precipitació de fosfomolibdat amònic.
Aquesta prova convé fer-la una vegada sabem que la prova dels arsenats ha estat negativa, ja que aquests també podrien donar un precipitat d’un color similar encara que menys intens.
7- Clorurs/Iodurs
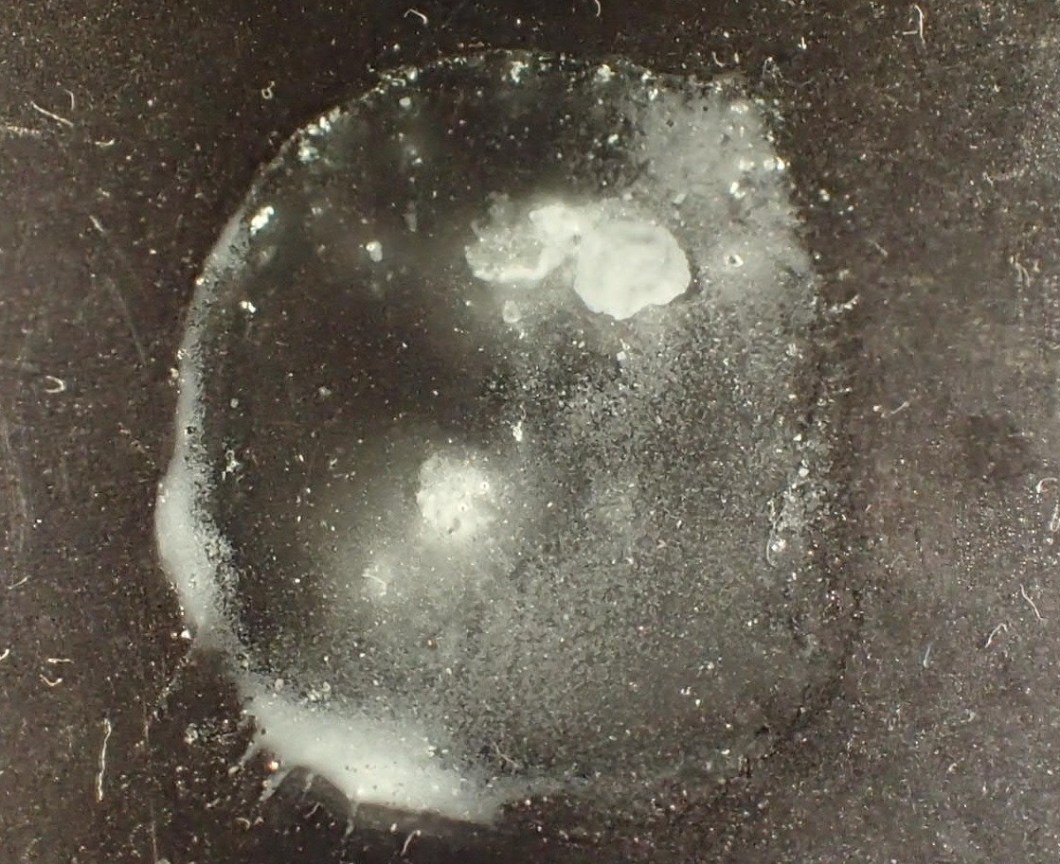
Com en el cas del fosfat, prepararem la dissolució submergint la mostra en àcid nítric. A continuació, prepararem una petita dissolució de nitrat de plata en aigua destil·lada. Finalment deixarem anar una o dues gotes de la dissolució de nitrat de plata en la dissolució de la mostra. En el cas que a la nostra dissolució hi hagi clor, veurem ràpidament com es forma una pasta blanca degut a la precipitació de clorur de plata. És molt important fer servir aigua destil·lada, donat que el clor de l’aigua de l’aixeta seria suficient per tornar la solució de color blanc.

Si la pasta, en lloc de blanca, agafa un color més aviat groguenc, es tractarà amb molta probabilitat d’un iodur. Si tenim dubtes de si es tracta d’un clorur o d’un iodur, podem afegir una o dues gotes d’amoníac a la dissolució. Si el precipitat es dissol, ens confirmaria que es tracta d’un clorur; si, pel contrari, el precipitat no experimenta cap canvi, significarà que es tracta d’un iodur, completament insoluble en amoníac.
8- Fluorurs
Per determinar si la nostra mostra és un fluorur, submergirem un trosset en àcid clorhídric fins que es dissolgui. Per altra banda, preparem una altra solució d’àcid clorhídric (HCl) amb una mica de pols de calcita (CaCO3), que es dissoldrà en el clorhídric produint la típica efervescència. Seguidament, afegim una o dues gotes de la dissolució amb calcita en la de la mostra. Si la nostra mostra conté l’anió fluorur, es produirà un precipitat cristal·lí entre incolor i blanc degut a la formació de fluorita (CaF2) segons la reacció:
CaCO3 + 2 HF → CaF2 + CO2 + H2O
S’ha de dir que no trobarem molts fluorurs solubles en àcid clorhídric (HCl). En lloc de fer servir clorhídric, aquesta prova també es pot fer amb àcid sulfúric concentrat (H2SO4) amb el que els fluorurs, en general, presenten millor dissolució.
9- Nitrats/borats de sodi
Encara que el nombre de nitrats a la natura és força reduït, si la nostra mostra es dissol en aigua i no ha donat positiu en cap de les proves anteriors, és probable que es tracti d’un nitrat, ja que tots són solubles en aigua. Però hem de tenir en compte que dels grups d’anions que en general presenten bona solubilitat en àcids i que tinguin rellevància en nombre d’espècies a la natura, només els borats ens han quedat fora del nostre joc de proves. I d’aquests, fonamentalment els borats de sodi, com els nitrats, també acostumen a ser solubles en aigua a temperatura ambient.
Podem diferenciar si es tracta d’un borat afegint a la solució en aigua una gota d’una dissolució de clorur de bari, exactament com en la prova dels sulfats, de tal manera que si es produeix un precipitat blanc serà degut a la formació de borat de bari, insoluble en aigua.

Evidentment, aquestes proves s’han de poder complementar amb unes altres enfocades a la determinació de cations. Aquest tema és bastant més ampli i complicat, però sí que ha de ser possible el donar una relació de trucs/experiències que ens puguin ajudar a determinar el catió i, per tant, confio en que aquest només sigui el primer lliurament sobre la determinació de minerals mitjançant química analítica casolana.
Existeixen molts àmbits d’ajuda a la classificació dels minerals per mètodes casolans, fent servir analítica química o qualsevol altre mètode d’explotació de les propietats dels minerals. Com a exemple, al magnífic article de l’Adolf Cortel sobre el pleocroisme, publicat recentment, veiem com es podia estudiar el pleocroisme dels minerals amb un binocular i un simple polaritzador fotogràfic. Així que aprofito per animar-vos a compartir a Infominer els vostres coneixements, experiències i trucs que ens puguin ajudar en un tema tan apassionant com és la identificació dels minerals.
Bibliografia:
ARRIBAS JIMENO, S.; HERNÁNDEZ MÉNDEZ, J.; LUCENA CONDE, F.; BURRIEL MARTI, F. Química analítica cualitativa.
TREADWELL, F.P. Tratado de química analítica. Tomo I. AnálisisCualitativo.
Mineralienatlas https://www.mineralienatlas.de/index.php?lang=en&language=english
Un especial agraïment a en Carles Díez pel seu assessorament tècnic i la facilitació de documentació.